objectifs
Reconnaître et évaluer une douleur aiguë et une douleur chronique (douleurs nociceptives, neuropathiques et dysfonctionnelles) chez l’adulte et la personne âgée/peu communicante.
La douleur est définie par l’Association internationale pour l’étude de la douleur (IASP) comme « une expérience sensorielle et émotionnelle désagréable associée à une lésion tissulaire réelle ou potentielle ou décrite en ces termes ». Cette définition associe donc à la dimension sensorielle de la douleur d’un patient des dimensions affectives, psychologiques et émotionnelles qui lui sont propres. C’est donc une expérience subjective, difficile à qualifier et quantifier car fondée sur le ressenti propre d’une personne. L’expression d’une plainte douloureuse ne doit jamais être minimisée par des professionnels de santé car ils risquent alors d’en sous-évaluer le retentissement sur la vie du patient.
L’entretien avec un patient douloureux a donc deux objectifs simultanés : faire un diagnostic précis de l’origine de la douleur et évaluer son retentissement physique, émotionnel ou fonctionnel sur la vie quotidienne du patient.
Une difficulté supplémentaire de cet entretien vient du fait que la douleur n’est pas toujours en lien avec une lésion tissulaire de l’organisme. Le système nerveux nociceptif repose en effet sur une architecture dynamique de transmission et de modulation de l’information jusqu’au cortex cérébral. La dysfonction d’une ou de plusieurs étapes de traitement de cette information sensorielle n’a donc pas forcément la même sémiologie. La bonne connaissance des bases neurophysiologiques de la douleur est donc un prérequis pour une bonne évaluation clinique de celle-ci.
Neurophysiologie de la douleur
Anatomie du système nociceptif
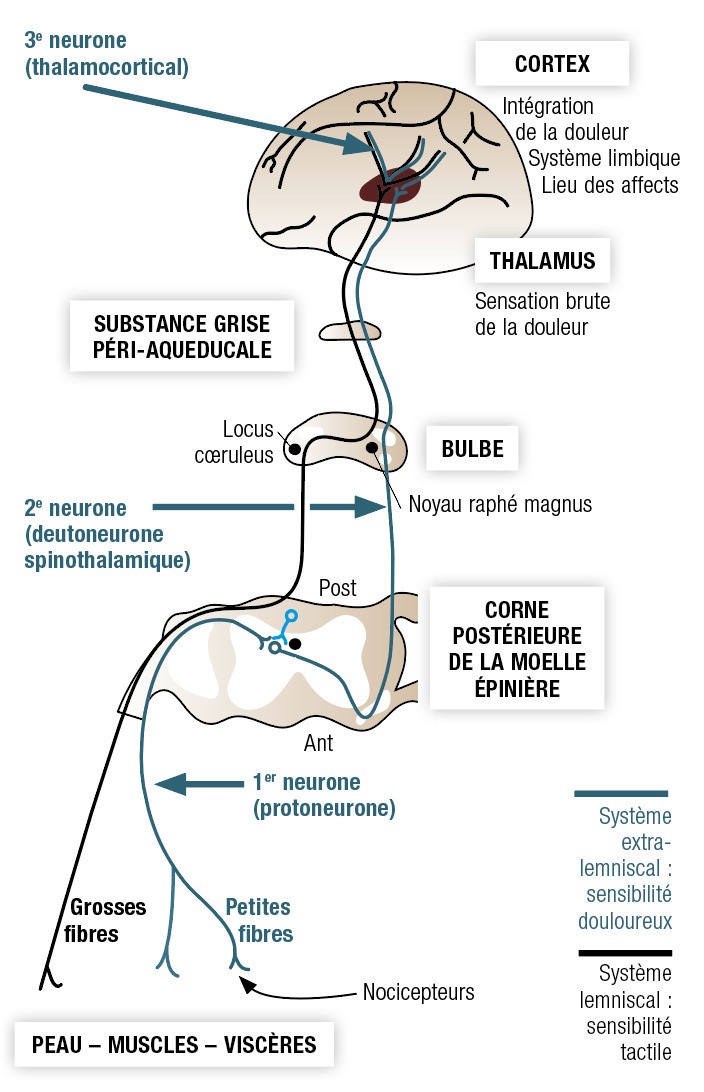
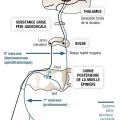
La douleur est une information sensorielle ascendante véhiculée de la périphérie de l’organisme (terminaisons sensitives libres, cutanées ou viscérales) jusqu’aux centres d’intégration cérébraux. Son organisation anatomique respecte donc l’organisation générale du système somato-sensoriel en 3 niveaux (fig. 1) avec :
- un protoneurone, neurone périphérique en T dont le noyau est dans le ganglion spinal. Son dendrite véhicule l’information du récepteur sensitif du territoire périphérique innervé par le nerf. La vitesse de conduction de l’information afférente dépend du diamètre et de la présence d'une gaine de myéline (tableau 1). Son axone fait synapse au niveau central dans la corne dorsale de la moelle ipsilatérale ;
- un deutoneurone, neurone entièrement situé dans le névraxe. Il est issu de la synapse médullaire et après décussation (franchissement de la ligne médiane dans la commissure blanche antérieure en avant du canal épendymaire) à son étage médullaire de naissance, il va cheminer au sein du faisceau antérolatéral de la moelle (ancien nom : faisceau spinothalamique). La voie antérolatérale va conduire l’information nociceptive de l’étage rachidien correspondant à travers les 3 étages du tronc cérébral jusqu’au thalamus ;
- un troisième neurone thalamocortical, qui s’articule avec le précédent à partir du thalamus (noyau ventro-postéro-latéral pour le corps hors région cervicale, noyau ventro-postéro- médian pour la région cervicale et céphalique). Ces noyaux du thalamus sont des relais où convergent l’ensemble des voies somesthésiques de l’organisme. À cet endroit s’effectue une intégration de l’information nociceptive avant sa projection par le troisième neurone sur les aires corticales somatosensorielles (circonvolution pariétale ascendante), rendant ainsi possible la localisation corporelle précise du stimulus d’origine. D’autres projections se font sur d’autres aires cérébrales (cortex préfrontal, cortex cingulaire antérieur, système limbique...) et expliquent ainsi la mémorisation ou le retentissement émotionnel du phénomène douloureux (v. Focus).
Système de contrôle descendant de la douleur
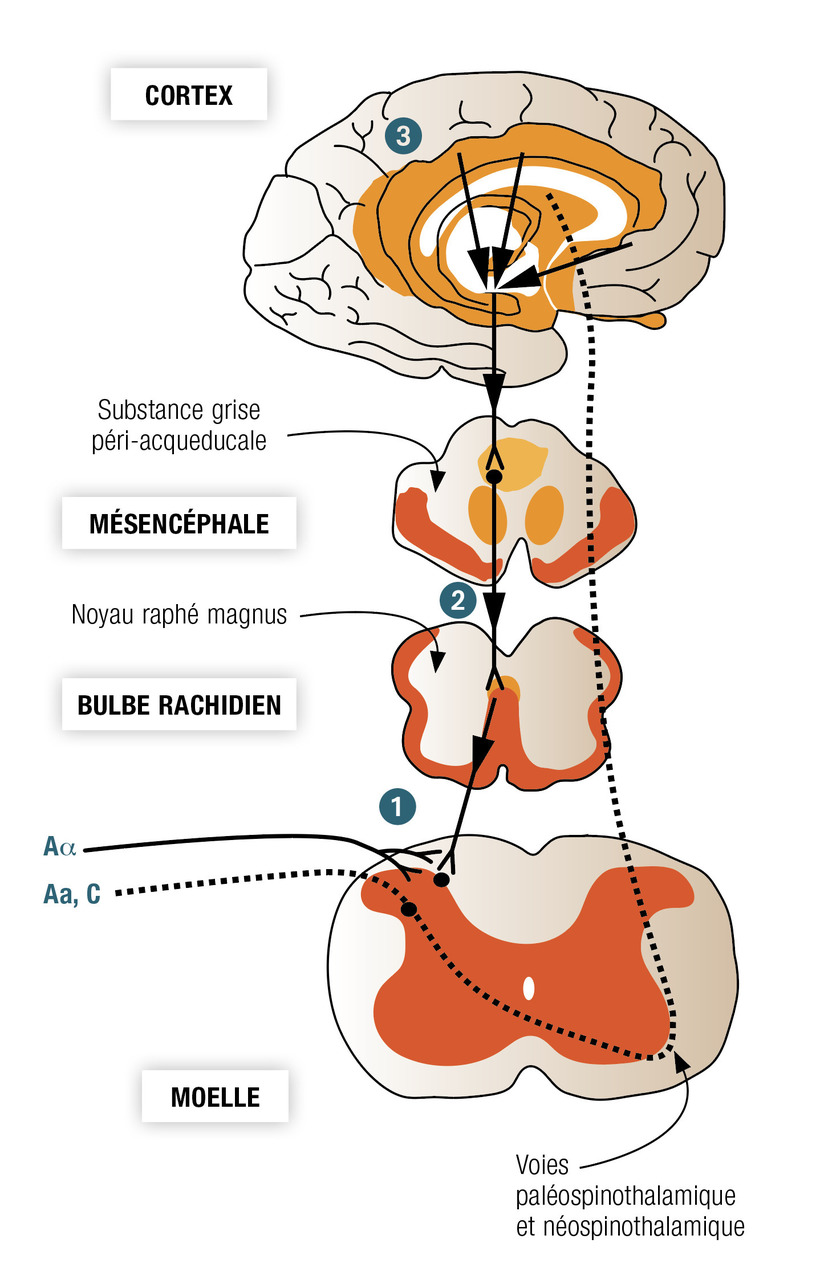
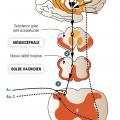
La perception douloureuse ne découle pas seulement de l’activation des voies nociceptives ascendantes mais d’un dialogue avec le système de contrôle descendant de la douleur. Ce contrôle fonctionne sur le mode d’un filtre qui module l’influx nociceptif aux différentes étapes de sa transmission ascendante. Ceci permet un véritable système de rétrocontrôle de la douleur (fig. 2) commandé par le cortex et le mésencéphale.
Comme pour l’anatomie des voies ascendantes, ce système de modulation est segmenté en 3 parties où chaque segment peut être modulé par les étages supérieurs :
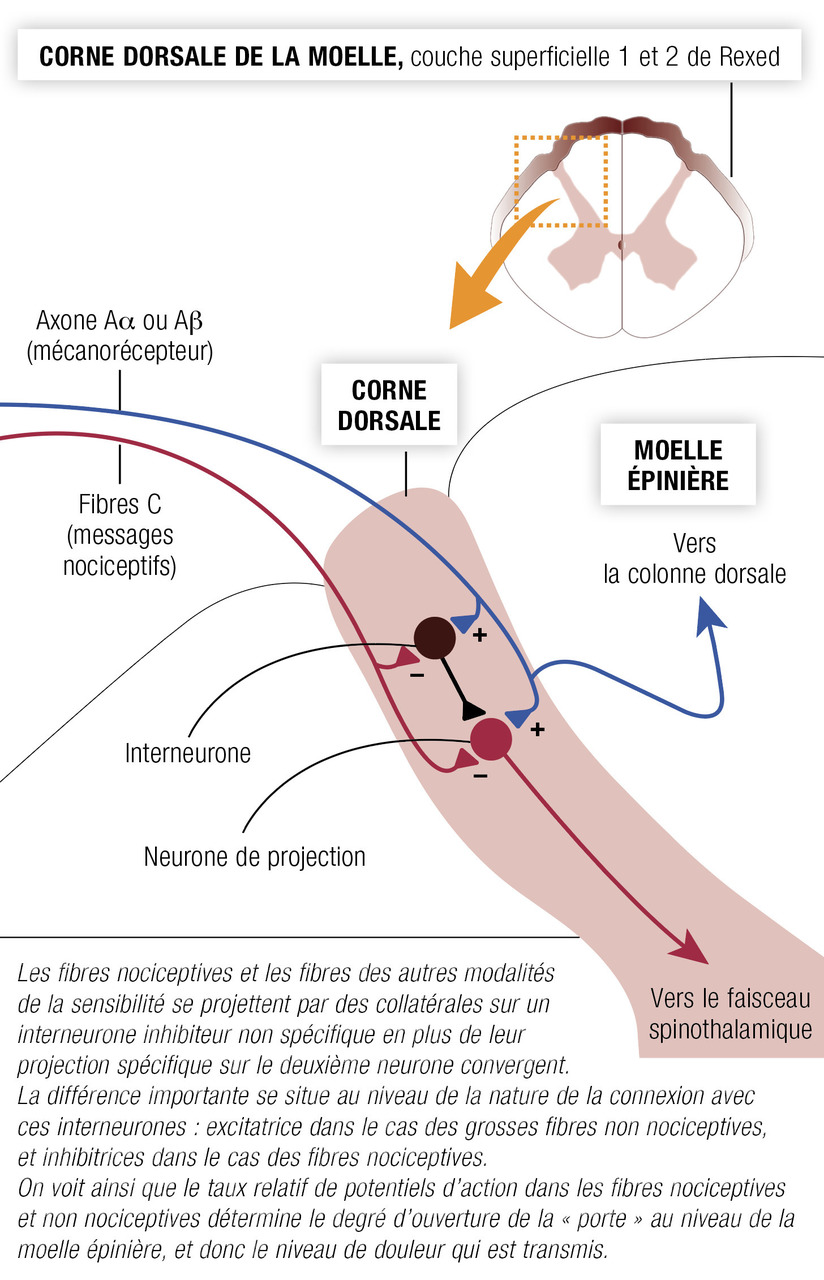
- le premier palier de ce contrôle est médullaire (fig. 3) et repose sur la théorie du gate control de Wall et Melzack (1965). Il s’agit du contrôle segmentaire de la douleur, présent à chaque étage dans la corne dorsale médullaire ;
- le deuxième palier est représenté par le contrôle inhibiteur diffus induit par des stimulations nociceptives (CIDN). Les afférences nociceptives ascendantes spinothalamiques ne font pas que transmettre le signal nociceptif au cortex cérébral. Le faisceau antérolatéral lors de sa traversée du mésencéphale et du tronc cérébral fait des connexions avec la substance grise périaqueducale et le noyau du raphé magnus. Ces noyaux vont émettre des efférences descendantes vers les interneurones segmentaires inhibiteurs médullaires. Ce système s’active lorsque deux stimulations douloureuses d’intensité différente sont appliquées à deux territoires distincts puisque le sujet ne perçoit que la douleur la plus intense. Le masquage d’une des douleurs vient de l’activation du contrôle inhibiteur diffus induit par les stimulations nociceptives qui facilite la transmission de l’influx nociceptif en « fermant la porte » (gate control) aux autres informations sensitives des segments médullaires.
- le troisième palier est le contrôle descendant d’origine corticale. L’hypnose ou l’effet placebo montre que la réponse corticale à l’intégration du phénomène douloureux peut diminuer la perception douloureuse. L’étude en imagerie fonctionnelle montre que les régions du cortex préfontral dorsolatéral et du cortex cingulaire antérieur peuvent activer la substance grise périaqueducale et recruter le contrôle inhibiteur diffus induit par les stimulations nociceptives en réponse à une douleur.
Physiologie de la douleur
Le changement de paradigme induit par la découverte des systèmes du contrôle de la douleur a amené à faire évoluer le modèle du fonctionnement des circuits nociceptifs. Ainsi est-on passé d’un modèle relativement linéaire de transmission de l’information afférente à un modèle circulaire de régulation.
L’influx nociceptif est soumis à 4 étapes pour être intégré en perception douloureuse.
La première étape est celle de la transduction, processus de conversion d’un stimulus chimique, thermique ou mécanique périphérique en activité électro-physiologique dans le protoneurone nociceptif.
La transmission représente la conduction de l’influx nociceptif au sein des voies anatomiques précédemment décrites.
À tous les niveaux de conduction de cette information sensorielle, celle-ci est soumise à une modulation constante. L’action de mécanismes excitateurs ou inhibiteurs va aboutir à une augmentation ou à une réduction de l’activité neuronale dans le système nociceptif et donc à une perception douloureuse plus ou moins intense. Un défaut de régulation de ces mécanismes peut jouer un rôle dans la chronicisation d’un phénomène douloureux.
Enfin, le processus final est l’intégration corticale de l’influx nociceptif. À l’étage cortical, l’influx nociceptif est intégré par la neuromatrice de la douleur, ce qui confère à l’expérience douloureuse les caractéristiques sensorielles, affectives et cognitives.
Une dysfonction de n’importe laquelle des étapes de ce modèle peut donc amener le patient à expérimenter une douleur très forte, non proportionnée à la lésion, voire à la chroniciser, et ce malgré la cicatrisation du processus lésionnel initiateur.
Douleurs aiguë et chronique
La distinction entre douleur aiguë et douleur chronique est importante car les approches sont très différentes : confondre ces deux tableaux peut conduire à de graves erreurs de prise en charge.
Douleur aiguë
La douleur aiguë est un signal d’alarme qui protège l’organisme. C’est un symptôme souvent utile dont il faut rapidement déterminer l’origine et la nature afin de mettre en œuvre le traitement adapté à la suppression de la cause (si possible) et à la disparition complète de la douleur. Comme dans toute douleur, une composante affective intervient sous la forme de manifestations anxieuses.
Douleur chronique
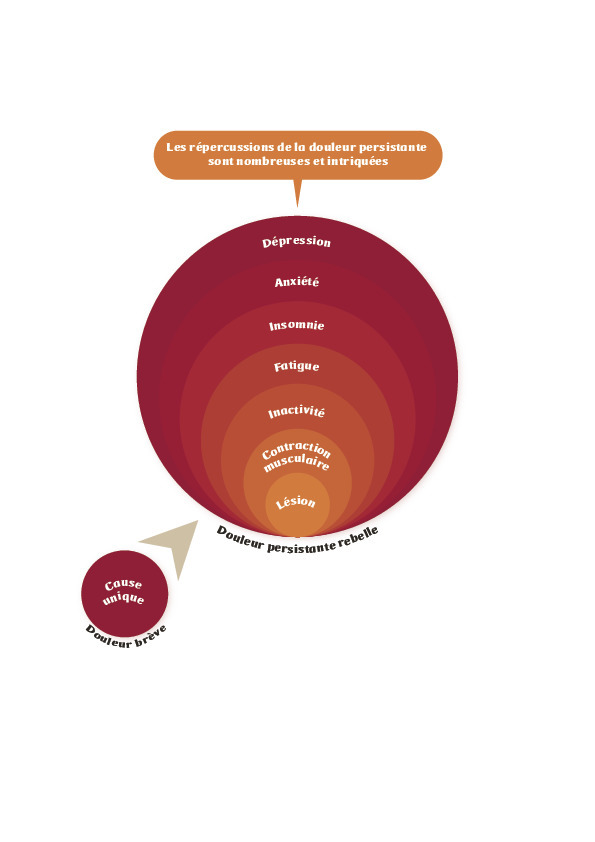
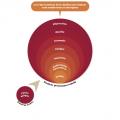
La douleur est chronique si sa durée est supérieure à 3 ou 6 mois. Ce n’est plus un symptôme mais un syndrome, plurifactoriel et complexe, associant des manifestations physiques mais également psychiques, comportementales et sociales (fig. 4). La douleur a perdu sa valeur protectrice pour devenir destructrice de la santé.
Cette évolution s’explique par des modifications structurelles du système nerveux central induites par une stimulation douloureuse prolongée (mémoire de la douleur). La douleur n’est plus contrôlée et d’ailleurs plus contrôlable par les seuls médicaments et elle envahit progressivement tout l’univers psychologique, affectif, cognitif et social du patient (c’est la maladie douloureuse chronique).
Douleurs aiguë et chronique intriquées
Il existe des tableaux douloureux associant une problématique de douleurs aiguës et de douleurs chroniques. Il s’agit essentiellement des douleurs cancéreuses dont l’intensité, les conditions de survenue se rapprochent plus de douleurs aiguës persistantes. Elles peuvent être associées à des séquelles de lésions anciennes responsables de douleurs plutôt chroniques. L’apparition, de par l’évolution de la maladie, de nouvelles douleurs est à prendre en compte comme des douleurs aiguës. Les maladies inflammatoires sévères et chroniques peuvent également être responsables de tableaux associant douleur aiguë et chronique.
Le choix d’une stratégie thérapeutique devant une douleur chronique nécessite toujours une évaluation minutieuse de la situation, souvent un avis pluridisciplinaire et ne relève donc pas de l’urgence.
Le traitement rapide et adapté de la douleur aiguë diminue le risque d’évolution vers un syndrome douloureux chronique. Il s’agit d’une urgence thérapeutique tant pour des raisons éthiques que pronostiques.
Sémiologie de la douleur
Les différentes atteintes du système nociceptif expliquent les différentes présentations cliniques rapportées par un patient.
Douleurs par excès de nociception/inflammatoires
Les douleurs par excès de nociception sont provoquées par la stimulation excessive des récepteurs nociceptifs périphériques lors d’une lésion tissulaire, d’une inflammation, d’une stimulation mécanique, thermique ou chimique. C’est là le mécanisme habituel d’activation des voies nociceptives qui survient après dommage des tissus périphériques (coup de marteau sur le pouce, par exemple). La lésion tissulaire induit en effet le relargage périphérique de substances pro-algogènes (prostaglandines, ions H+, substance P...) qui vont se fixer sur les récepteurs canaux des fibres nociceptives périphériques et les activer.
Ces douleurs ont une topographie non systématisée correspondant au territoire où se produit la stimulation et s’accompagnent de réactions végétatives (sudation, élévation tensionnelle, tachycardie...). Un cas particulier est représenté par les douleurs viscérales projetées ou référées (douleur du bras gauche après un infarctus du myocarde, par exemple). Ceci s’explique par une convergence des neurones sensoriels viscéraux avec les neurones nociceptifs périphériques au sein des couches de Rexed de la corne médullaire. Le cortex analyse la douleur viscérale comme une douleur sur le dermatome innervé par le segment médullaire périphérique correspondant.
Le traitement de ces douleurs passe donc par la suppression ou la diminution du stimulus nociceptif et par l’administration d’antalgiques à différents endroits au niveau périphérique et/ou central.
Douleurs neuropathiques
Contrairement aux douleurs par excès de nociception, certaines douleurs s’expriment en l’absence de stimulation périphérique. Ce sont les douleurs neuropathiques, toujours associées à une lésion du système nerveux périphérique ou central. La topographie de la douleur sera systématisée selon la localisation de cette lésion.
L’examen neurologique retrouve fréquemment un déficit dans le territoire correspondant. Le patient décrit souvent des douleurs continues à type de brûlures, ainsi qu’une composante plus paroxystique en « décharge électrique », ce qui permet un dépistage avec un outil adapté, le DN4 (tableau 2). Un cas typique de cette douleur est présent chez des patients amputés (douleur du « membre fantôme »).
Il existe des liens entre douleurs par excès de nociception et douleurs neuropathiques. Ainsi, une des conséquences des médiateurs algogènes est de sensibiliser les fibres nociceptives périphériques. Elles émettent alors des potentiels d’action pour des stimulations faibles voire absentes, et ce même après la cicatrisation du processus lésionnel ou l’arrêt de l’exposition aux substances inflammatoires. En clinique, les patients présentent une allodynie (réponse douloureuse à un stimulus non douloureux) ou une hyperalgésie (réponse exagérée à un stimulus douloureux de faible intensité).
Ces mêmes phénomènes de sensibilisation se retrouvent au niveau central. Ainsi, un accident vasculaire cérébral thalamique ou une atteinte démyélinisante au cours d’une sclérose en plaques peuvent aussi déséquilibrer les systèmes de contrôle descendant de la douleur. Ceci rend le système du gate control médullaire inopérant et renforce le stimulus douloureux.
Ces douleurs ne répondent que peu aux antalgiques conventionnels et nécessitent une approche mêlant antiépileptiqueet/ou antidépresseur.
Douleurs dysfonctionnelles
Le dernier type de douleur est la douleur dysfonctionnelle. Elle ne résulte a priori ni d’une inflammation ni d’une atteinte neurologique évidente. Elle serait liée à un dysfonctionnement des mécanismes descendants de contrôle de la douleur ou de son intégration. Cette absence de filtre rend les sujets plus sensibles aux stimuli douloureux ou non douloureux.
Ces douleurs se localisent à différents endroits du corps, fluctuent au cours du temps, sans correspondance lésionnelle. Elles restent donc un diagnostic d’exclusion et peuvent tromper le clinicien devant la multiplicité des présentations parfois intriquées (fibromyalgie, côlon irritable, stomatodynie...). Toute douleur physique ayant inévitablement un retentissement sur le psychisme de l’individu, il arrive parfois que la comorbidité dépressive soit au premier plan dans ces tableaux douloureux.
Évaluation d’une douleur
Lors de l’évaluation d’un patient douloureux, le praticien doit s’attacher à recueillir l’ensemble des informations pertinentes sur la symptomatologie douloureuse pour guider la prise en charge et le suivi. Ainsi l’anamnèse et l’examen clinique doivent permettre d’identifier la nature de la symptomatologie douloureuse et de faire le lien avec l’existence d’une lésion parfois cicatrisée depuis longtemps. L’évaluation s'attache également à mesurer le retentissement émotionnel et le retentissement sur la qualité de vie du patient à partir d’outils spécifiques. Enfin, à l’issue de l’entretien, le praticien fait une synthèse des aspects de la douleur du patient pour adapter son suivi aux problématiques du patient.
Dans un contexte de douleur aiguë, l’interrogatoire et l’examen clinique initial doivent être très rapides, centrés sur l’origine de la douleur et son intensité afin d’orienter et surtout ne pas retarder la mise en place d’un traitement antalgique adapté. Une fois le patient soulagé, l’interrogatoire et l’examen clinique seront repris afin de mieux analyser la lésion responsable de la douleur et éventuellement proposer un traitement étiologique plus spécifique.
Au contraire, l’approche d’un patient douloureux chronique est beaucoup plus longue et complexe. Il faudra dans un premier temps laisser le patient exprimer sa douleur selon ses propres mots qui ont souvent une valeur diagnostique irremplaçable et être attentif à des éléments de communication non verbale ainsi qu’à une éventuelle discordance entre la présentation générale, les mouvements, l’attitude du patient et la plainte douloureuse.
Anamnèse de la douleur
Il faut systématiquement rechercher les informations suivantes :
- biographie du patient sur le plan médical (antécédents médicaux, chirurgicaux, obstétricaux, psychiatriques et familiaux) ;
- circonstances de déclenchement de la douleur ;
- modalités de la prise en charge initiale ;
- description de la douleur initiale (topographie, type de douleur, intensité) ;
- contexte personnel, familial, professionnel, social dans lequel la douleur est intervenue ;
- évolution du tableau douloureux, notamment en fonction des différents médicaments et prises en charge médicales. Insistons sur la nécessité d’un interrogatoire poussé à ce sujet : il ne s’agit pas uniquement de savoir quel traitement a été administré mais à quelles doses et pendant combien de temps ;
- description de la douleur actuelle (topographie, type de douleur, intensité), profil évolutif sur le nycthémère et le long terme, facteurs d’aggravation et de soulagement ;
- retentissement sur la qualité de vie, sur le sommeil, sur les activités personnelles, professionnelles… ;
- situation actuelle du patient sur le plan familial, professionnel et socio-économique, existence de procédures judiciaires, sociales ou administratives en cours.
Il faut également rechercher tous les événements de la vie du patient qui pourraient avoir une place, un sens dans la douleur actuelle, en s’intéressant particulièrement aux traumatismes de tous ordres (agressions physiques ou psychiques, éventuellement à caractère sexuel, deuils…).
Échelles d’évaluation
Comme l’expression de la douleur est un symptôme subjectif et que son expression varie selon les patients, il existe des outils simples et validés qui simplifient son suivi et permettent d’objectiver des changements après intervention thérapeutique.
On privilégie toujours en première intention les outils d’auto- évaluation. Ils permettent au patient d’exprimer sa douleur selon ses propres références. Ils facilitent le suivi car l’outil est standardisé et reproductible au cours du temps, une modification de sa cotation permet donc au praticien d’objectiver un changement dans la symptomatologie.
En cas d’impossibilité de communication, on utilise des échelles d’hétéro-évaluation. Elles permettent généralement de ne pas négliger une manifestation douloureuse dans des situations complexes (coma, démence...). L’examinateur s’appuie sur les modifications du langage corporel, du comportement et de l’attitude du patient pour objectiver indirectement l’existence de la douleur.
Enfin, les échelles d’évaluation sont classées selon le nombre d’informations ou de dimensions de la douleur qu’elles évaluent. Certaines comme l’échelle visuelle analogique (EVA) ne font que quantifier l’intensité de la douleur, ce qui n’informe pas sur la qualité de celle-ci (neuropathique, nociceptive...) et ne peut donc pas servir au diagnostic étiologique de la douleur. D’autres, au contraire, pour orienter le praticien, mêlent des adjectifs qualificatifs de la symptomatologie douloureuse à des échelles de retentissement psychologique. Elles sont alors qualifiées de multidimensionnelles.
Échelles unidimensionnelles
Elles mesurent globalement l’intensité de la douleur ; ces échelles d’auto-évaluation (utilisées directement par le patient) sont simples, reproductibles, fiables et validées.
On distingue :
- l’échelle numérique (EN), qui permet au patient de donner une note de 0 à 10 ; la note 0 est définie par « pas de douleur » et la note 10 par « douleur maximale imaginable » ;
- l’échelle verbale simple (EVS), qui comporte une série de qualificatifs hiérarchisés, pouvant être adaptés au patient et décrivant l’intensité de la douleur (« absente » = 0, « faible » = 1, « modérée » = 2, « intense » = 3, « extrêmement intense » = 4) ;
- l’échelle visuelle analogique (EVA), réglette avec une ligne horizontale de 100 mm, orientée de gauche à droite. Les deux extrémités sont présentées comme « pas de douleur » et « douleur maximale ». Le patient évalue sa douleur en déplaçant un curseur sur la ligne. Au dos de la réglette, la graduation permet de chiffrer la position du curseur et donc l’intensité de la douleur de 0 à 100 mm.
L’objectif de ces outils est d’orienter l’examen clinique et l’interrogatoire dans un contexte de douleur aiguë afin de ne pas retarder la mise en place d’un traitement spécifique. Ils n’apportent aucune autre information sur la nature et le mécanisme de la douleur et ont donc une implication limitée aux choix des thérapeutiques
Échelles comportementales
Ces échelles s’intéressent aux patients incapables de communiquer (intubation en réanimation, patient cérébrolésé, patient dément...). L’examinateur est un tiers qui observe en hétéro-évaluation son patient. Elles sont donc des outils de 2e intention à appliquer après échec de l’autoévaluation.
Nous détaillons ici succinctement les échelles utilisées en gériatrie qui correspondent chacune à une situation spécifique.
L’échelle Algoplus est utilisée dans les services d’accueil d’urgence. Elle est constituée de 5 items (visage, regard, plaintes, corps, comportements). L’observation d’un seul comportement correspondant à un des items implique sa cotation par le soignant. Chaque item coté « oui » vaut 1 point. Le soignant doit ensuite additionner les points pour obtenir un résultat sur 5. Un score supérieur ou égal à 2 signale la présence d’une douleur.
L’échelle Doloplus est utilisée dans les services d’hospitalisation conventionnelle gériatrique. Elle est destinée aux sujets âgés présentant des difficultés d’expression, des troubles de la mémoire ou encore des troubles cognitifs. Elle se compose de 10 items répartis en 3 groupes (retentissement somatique, psychomoteur, psychosocial). La cotation de chaque item se situe entre 0 et 3 et le score total est compris entre 0 et 30. Un score de 5 sur 30 manifeste la présence de la douleur.
L’échelle comportementale pour personne âgée (ECPA) est utilisée en gériatrie chez des personnes présentant des troubles de la parole pour évaluer la douleur induite par les soins. Cette échelle comporte 8 items (visage, position au repos, mobilité du patient, relation à autrui, anticipation des soins, réaction à la mobilisation, réaction aux soins des zones douloureuses et plaintes pendant les soins) comprenant chacun 5 possibilités, cotées de 0 à 4. Le score total est compris entre 0 et 32 et va d’une absence de douleur à une douleur totale. L’observation du patient par le soignant, laquelle aboutira à la cotation, se réalise en deux temps. La première partie a lieu impérativement 5 minutes minimum avant le soin, la seconde a lieu après le soin.
Échelles multidimensionnelles
Plus complexes que les échelles globales unidimensionnelles, ces outils se présentent comme des outils de recherche. Ils permettent d’offrir la possibilité d’une évaluation à la fois quantitative et qualitative de la douleur et en particulier de sa composante sensorielle et affective, ainsi que de son retentissement sur la vie quotidienne du patient. Ce type de questionnaire ne se prête pas à des mesures répétées mais est adapté à des passations plus espacées, pour la douleur chronique par exemple.
Il en existe de différentes qui permettent de préciser certains aspects du syndrome douloureux chronique. Ainsi l’échelle de Saint-Antoine est un questionnaire d’adjectifs qui oriente sur de possibles mécanismes de la douleur. On peut le compléter avec l’échelle de dépistage de la dépression et de l’anxiété HAD (hospitalisation anxiety and depression scale) ou des échelles d’évaluation du retentissement sur la qualité de vie, type SF 36. Le médecin doit veiller à ne pas remplacer son interrogatoire par une utilisation excessive des échelles, ce qui limiterait alors la parole du patient. Ce sont des outils de dialogue, d’échanges, à intégrer dans sa pratique.
Conclusion
Conduire l’entretien avec un patient douloureux se fonde sur une bonne compréhension des mécanismes neurophysiologiques et sur leur poids respectif dans l’architecture du phénomène douloureux. Le but de l’interrogatoire est de s’orienter sur le mécanisme lésionnel sous-jacent avant de le confirmer par l’examen clinique. L’évaluation du retentissement est nécessaire pour proposer une prise en charge personnalisée et adaptée au quotidien du patient. Cette évaluation globale du diagnostic au retentissement utilise des outils spécifiques afin de pouvoir s’adapter à n’importe quelle situation clinique. Elle s’impose à tout soignant pour le suivi du soulagement du patient ainsi que son information dans un souci d’éducation thérapeutique.
La perception douloureuse est la résultante du dialogue entre la transmission afférente de la nociception et la modulation par les systèmes de contrôle descendant.
La douleur aiguë est un symptôme à soulager rapidement pour éviter les remaniements neurophysiologiques responsables de l’entretien du syndrome douloureux chronique.
Il existe trois grands types de douleur : par excès de nociception, neuropathique et la douleur dysfonctionnelle.
L’examen d’un patient douloureux a deux objectifs : faire le bilan étiologique lésionnel et évaluer le retentissement global de sa douleur sur sa vie quotidienne.
Les outils d’évaluation de la douleur sont à utiliser dans des indications précises et doivent être intégrés dans le suivi du patient.
Message de l'auteur
L’item 131 est un item riche en notions théoriques et fondamentales. Dans l’idée de dossiers transversaux, il s’articulera avec l’item 132 sur les thérapeutiques et ne concernera que quelques questions du dossier.
La douleur nociceptive peut concerner un dossier de traumatologie, d’urgence ou de chirurgie.
La douleur neuropathique s’intègre généralement dans les dossiers de neurologie ou de médecine physique et réadaptation.
Un bon exemple de prise en charge de douleur dysfonctionnelle concerne la lombalgie chronique.
Enfin, la maladie cancéreuse est une situation typique qui permet de faire cohabiter douleur aiguë et chronique, ainsi que ces caractéristiques nociceptives ou neuropathiques.
Il pourrait être demandé :
de distinguer douleur aiguë et chronique ;
d’identifier et justifier le caractère neuropathique (DN4) ;
de faire le lien entre douleur neuropathique et atteinte lésionnelle correspondante ;
d’évaluer la douleur en citant une échelle spécifique de la douleur chez une personne âgée ;
de justifier l’efficacité d’un traitement selon les modifications de l’échelle numérique.
F. Jedryka déclare n’avoir aucun lien d’intérêts. P. Ginies déclare avoir participé à des interventions ponctuelles pour les entreprises Mundi Pharma, Grünenthal, Astellas ; et avoir été pris en charge, à l’occasion de déplacement pour congrès, par Mylan.
HAS. Recommandation de bonne pratique. Douleur chronique : reconnaître le syndrome douloureux chronique, l’évaluer et orienter le patient. Déc. 2008. http://www.has-sante.fr/portail/jcms/c_732257/fr/douleur-chronique-reconnaitre-le-syndrome-douloureux-chronique-l-evaluer- et-orienter-le-patient.
HAS. Recommandation en santé publique. Douleur chronique : les aspects organisationnels. Avril 2009. http://www.has-sante.fr/portail/jcms/c_813396/fr/douleur-chronique-les-aspects-organisationnels.
HAS. Recommandation de bonne pratique. Évaluation et suivi de la douleur chronique chez l'adulte en médecine ambulatoire. Fév 1999. http://www.has-sante.fr/portail/jcms/c_540915/fr/evaluation-et-suivi-de-la-douleur-chronique-chez-l-adulte-en-medecine-ambulatoire
Polycopié de neurologie. Collège des enseignants de neurologie, 2e cycle, item transversal douleur. www.cenneurologie.fr/2emecycle/Items inscritsdanslesmodulestransversaux/Douleurs/index.phtml
La Revue du Praticien, vol. 63. Peyron R. Physiopathologie de la douleur chronique et ses trois grands types. Juin 2013.
La Revue du Praticien, vol. 63. Serrié A. Évaluation du patient ayant une douleur chronique. Juin 2013.
Institut UPSA de la douleur. Item Outils d’évaluation de la douleur. http://www.institut-upsa-douleur.org/iudtheque/outils-evaluation-de-la-douleur

 Encadrés
Encadrés